Του Εμμανουήλ Μπιμπή,
Τα Mucorales αποτελούν τάξη νηματοειδών μυκήτων που συμπεριφέρονται ως ευκαιριακά παθογόνα, προκαλώντας λοιμώξεις του αναπνευστικού συστήματος σε συγκεκριμένες κατηγορίες ασθενειών. Η ασθένεια που προκαλούν ονομάζεται βλεννώδης μυκητίαση, ενώ στις ομάδες κινδύνου ανήκουν, εκτός από τα άτομα που βρίσκονται σε ανοσοκαταστολή ή αντικαρκινική θεραπεία για την αντιμετώπιση της λευχαιμίας, άτομα με συγκεκριμένα μεταβολικά σύνδρομα ή άτομα με επίκτητη ανοσοανεπάρκεια μετά από τραυματισμούς. Η αυξημένη ποσότητα σιδήρου στον ορό του αίματος ως αποτέλεσμα διάφορων παραγόντων, ανάμεσά τους η διαβητική κετοξέωση ή άλλης μορφής οξέωση, οδηγεί σε αυξημένη ευαισθησία απέναντι σε αυτήν την ασθένεια.
Όσον αφορά την θνησιμότητά της, κυμαίνεται από 50% ως και 70% ενώ σε περίπτωση εκτεταμένης λοιμώξεις στους πνεύμονες μπορεί να αγγίξει και το 90%. Παράλληλα, εμφανίζει μεγάλη νοσηρότητα και συχνά απαιτεί χειρουργική επέμβαση, αλλά και έμφυτη ανθεκτικότητα σε πολλά αντιμυκητιακά. Ο σίδηρος αποτελεί σημαντικό στοιχείο για τον κύκλο ζωής του μύκητα και επομένως τόσο ο ίδιος όσο και ο ξενιστής διαθέτουν τους κατάλληλους μοριακούς μηχανισμούς για την πρόσληψή του. Από την μεριά του μύκητα, η πρόσληψη του σιδήρου αποτελεί τμήμα της παθογονικότητάς του, ενώ από την μεριά του ξενιστή, η εξάντληση του σιδήρου από το περιβάλλον του μύκητα και συγκεκριμένα στο φαγόσωμα, περιορίζει την ανάπτυξή του και αποτελεί το nutritional immunity.
Η είσοδος του σιδήρου στο μύκητα διαμεσολαβείται από κατάλληλες πρωτεΐνες που ονομάζονται σιδηροφόρες και το δεσμεύουν σε μορφή ιόντος το οποίο αφού εισέλθει στο κύτταρο, απελευθερώνεται στο κυτταρόπλασμα. Παράλληλα, το κύτταρο διαθέτει περμεάσες, δηλαδή πολυπρωτεινικά σύμπλοκα στην μεμβράνη του κυττάρου, που επίσης συμμετέχουν στην είσοδό του. Ενδιαφέρον προκαλεί η ικανότητά του να χρησιμοποιεί σιδηροφόρες πρωτεΐνες από το περιβάλλον του, για να προσλάβει σίδηρο όπως συμβαίνει στην περίπτωση ασθενών που πραγματοποιούν αιμοκάθαρση και τους χορηγείται η σιδηροφόρα πρωτεΐνη DFO. Από την μεριά του ξενιστή, η ομοιόσταση του σιδήρου επηρεάζεται από την οξέωση, καθώς πρωτονιώνονται οι πρωτεΐνες που συμμετέχουν στην μεταφορά του, οδηγώντας σε αυξημένη ποσότητα στον ορό του αίματος.
Η αλληλεπίδραση μεταξύ του ανοσοποιητικού συστήματος του ξενιστή και του παθογόνου αποτελεί πεδίο έντονης έρευνας, καθώς οι ερευνητές προσπαθούν να αποκαλύψουν τους μοριακούς μηχανισμούς με τους τα φαγοκύτταρα εγκολπώνουν και καταστρέφουν στο εσωτερικό τους τα κονίδια του μύκητα και ταυτόχρονα το πως ο μύκητας μπορεί να αντισταθεί, να επιβιώσει και να παραμείνει στο εσωτερικό των φαγοκυττάρων.
Στα πλαίσια της έμφυτης-μη ειδικής άμυνας του οργανισμού, κεντρικό ρόλο για την αντιμετώπιση αεριογόνων μυκητιακών λοιμώξεων κατέχουν κυρίως τα μακροφάγα και τα ουδετερόφιλα. Οι μύκητες αυτοί είναι εξωκυττάρια παθογόνα αλλά φαίνεται να έχουν την δυνατότητα εφόσον φαγοκυττωθούν, να ξεφύγουν από το φαγόσωμα. Για την μελέτη όλων των παραπάνω, χρησιμοποιούνται ως μοντέλα της μόλυνσης ανοσοκατεσταλμένα ποντίκια στα οποία χορηγούνται μύκητες Rhizopus που ανήκουν στα Mucorales και Aspergillus, καθώς αποτελούν καλά μελετημένοι νηματοειδείς μύκητες που προκαλούν επίσης αναπνευστικές λοιμώξεις.
Αρχικά, μελετήθηκαν τα γενικά χαρακτηριστικά των αποκρίσεων του ανοσοποιητικού συστήματος απέναντι στα Mucorales. Βρέθηκε πως τα Rhizopus σε αντίθεση με τα Aspergillus μπορούσαν να παραμείνουν κυρίως στο εσωτερικό των κυψελιδικών μακροφάγων έως και δέκα μέρες μετά την χορήγηση, ενώ ιστολογικά δείγματα δείξανε την ανάπτυξη οιδήματος και την στρατολόγηση ουδετερόφιλων. Ο μύκητας στο εσωτερικό των κυττάρων βρίσκεται με την μορφή κονιδίων, δηλαδή σπορίων που εξυπηρετούν την επιβίωση σε αντίξοα περιβάλλοντα και διευκολύνουν την διάδοση του. Εκτός από τα παροικούντα μακροφάγα που είναι εγκατεστημένα στους πνεύμονες, στρατολογούνται ουδετερόφιλα, φλεγμονώδη μονοκύτταρα από την κυκλοφορία του αίματος που διαφοροποιούνται σε μακροφάγα και δενδριτικά κύτταρα.
Έπειτα, συγκρίθηκε η ικανότητα των Rhizopus με τα Aspergillus να φαγοκυττώνονται και να επιβιώνουν από μακροφάγα προερχόμενα από τον ερυθρό μυελό των οστών και ουδετερόφιλα. Σε επιβεβαίωση με προηγούμενα in vivo πειράματα, τα Rhizopus μπορούσαν να φαγοκυτταρωθούν κυρίως από τα μακροφάγα και σε μεγαλύτερο ποσοστό από τα Aspergillus. Η διαφορική ικανότητα επιβίωση των Mucorales εντός των μακροφάγων οδήγησε στον έλεγχο της ευαισθησίας των κονιδίων απέναντι στο οξειδωτικό στρες που προκαλούν τα μακροφάγα, μέσω του υπεροξειδίου του υδρογόνου και του μη οξειδωτικού στρες, μέσω επώασης με αυξανόμενες συγκεντρώσεις υδρολασών δηλαδή ενζύμων που διασπούν μακρομόρια από τα λυσοσσώματα. Τα αποτελέσματα έδειξαν συγκρίσιμη ευαισθησία σε αυτές τις συνθήκες.
Ένας κοινός μηχανισμός αποφυγής της λύσης των μυκήτων από τα μακροφάγα είναι η επαγωγή κυτταρικού θανάτου και άρα η απελευθέρωση από το εσωτερικό των κυττάρων. Και οι δυο μύκητες έδειξαν συγκρίσιμη ικανότητα να επάγουν απόπτωση ή νέκρωση στα μακροφάγα. Επομένως, τα Mucorales επιβιώνουν στο εσωτερικό των κυττάρων και συγκεκριμένα των φαγοσωμάτων αποφεύγοντας την λύση στα λυσοσσώματα.
Ο μηχανισμός με τον οποίο επιβιώνουν στο εσωτερικό των κυττάρων αποκαλύφθηκε όταν πραγματοποιήθηκε σύγκριση του σχηματισμού του φαγοσώματος κατά την φαγοκύτωση κονιδίων των δυο μυκήτων. Βρέθηκε πως τα Rhizopus μπορούσαν να εμποδίσουν την ενεργοποίηση ενός συγκεκριμένου μονοπατιού φαγοκύτωσης (LAP) που είναι κοινό κατά την δημιουργία του φαγοσώματος. Παράλληλα, η πρωτεΐνη Rab5, που στρατολογείτε στο φαγόσωμα στα αρχικά στάδια της ωρίμανση του, δεν βρέθηκε στα φαγοσώματα με τα Rhizopus. Επιπρόσθετα, αποδείχτηκε ότι εμποδίζεται η σύντηξη του φαγοσώματος με το λυσόσσωμα του κυττάρου.
Βασισμένοι σε προηγούμενα πειράματα που έδειξαν πως στο κυτταρικό τοίχωμα των ανενεργών κονιδίων του Aspergillus υπάρχει μελανίνη που προάγει την αναστολή της λύσης του μύκητα και η απομάκρυνση της οδηγεί σε εκκαθάριση του από το εσωτερικό του κύτταρου, αποκαλύφθηκε ο μοριακός μηχανισμός παραμονής και των Rhizopus. Η διατήρηση της μελανίνης στο κυτταρικό του τοίχωμα, λόγω έλλειψης αναδιαμόρφωσης και παραμονής σε ανενεργή κατάσταση, επιτρέπει την παραμονή στο εσωτερικό των μακροφάγων.
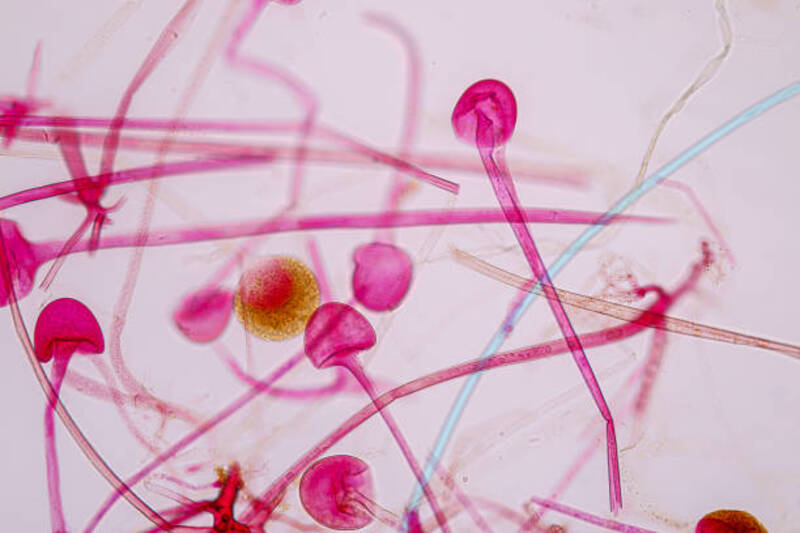
Όπως αναφέρθηκε πριν, ο σίδηρος αποτελεί σημαντικό στοιχείο για την ανάπτυξη του μύκητα και υπάρχει ένας διαρκής ανταγωνισμός μεταξύ αυτού και του ξενιστή για αυτόν. Παράλληλα, παρότι τα μακροφάγα δεν μπορούν να λύσουν τα ανενεργά κονίδια τα οποία βρίσκονται στο εσωτερικό, ενδεχομένως μπορούν να αναστείλουν την ανάπτυξή τους. Μεταγραφωματική μελέτη μέσω αλληλούχησης των αγγελιοφόρων RNA (mRNA) του ξενιστή και του μύκητα σε διαφορετικές χρονικές στιγμές, έδειξαν ότι από την μεριά των εκφράζονται περισσότερο γονίδια τα οποία κωδικοποιούν πρωτεΐνες για την αφομοίωση του σιδήρου και αντίστοιχα στον μύκητα επάγονται γονίδια για την πρόσληψη σιδήρου σε συνθήκες έλλειψής του από το περιβάλλον.
Η άμεση επίδραση του σιδήρου στη ανάπτυξη των κονιδίων εντός των μακροφάγων δείχτηκε όταν μολύναμε μακροφάγα με κονίδια παρουσία ή μη σιδήρου. Βρέθηκε πως μόνο όταν υπήρχε σίδηρος, μπορούσε ο μύκητας να βλαστάνει, να προκαλέσει λύση του μακροφάγου και άρα κυτταρικό θάνατο δώδεκα ώρες μετά την αρχική μόλυνση.
Συνοψίζοντας, οι αναπνευστικές λοιμώξεις που προκαλούνται από τα Mucorales αποτελούν απειλή για έναν όλο και μεγαλύτερο αριθμό ανοσοκατεσταλμένων ασθενών ή ασθενών με μεταβολικά νοσήματα. Η υψηλή του θνησιμότητα και νοσηρότητα, καθώς και η έμφυτη ανθεκτικότητά του σε πολλά αντιμυκητιακά απαιτεί σε βάθος κατανόηση της αλληλεπίδρασής του με το ανοσοποιητικό σύστημα με στόχο την ανάπτυξη αποτελεσματικών θεραπειών.
ΕΝΔΕΙΚΤΙΚΕΣ ΠΗΓΕΣ
- Iron restriction inside macrophages regulates pulmonary host defense against Rhizopus species, nature.com. Διαθέσιμο εδώ
- Aspergillus Cell Wall Melanin Blocks LC3-Associated Phagocytosis to Promote Pathogenicity, cell.com. Διαθέσιμο εδώ
- Calcium sequestration by fungal melanin inhibits calcium–calmodulin signalling to prevent LC3-associated phagocytosis, nature.com. Διαθέσιμο εδώ