Της Σοφίας Μάντη,
Οι κακοήθεις νεοπλασματικές παθήσεις, που κοινώς αποκαλούμε καρκίνο, προσβάλλουν ετησίως εκατομμύρια ανθρώπους και ήταν το δεύτερο συχνότερο αίτιο θανάτου για το 2023. Εδώ και δεκαετίες, οι εδραιωμένες θεραπευτικές επιλογές περιλαμβάνουν τη χειρουργική επέμβαση, τη χημειοθεραπεία και την ακτινοθεραπεία. Λόγω των υψηλών ποσοστών νοσηρότητας και θνησιμότητας, η επιστημονική κοινότητα αναζητά συνεχώς νέες λύσεις για την αντιμετώπισή τους και τα τελευταία χρόνια φαίνεται πως οι προσπάθειες αποδίδουν καρπούς. Η ανοσοθεραπεία αποτελεί μια νέα θεραπευτική προσέγγιση, η οποία λειτουργεί ενεργοποιώντας ή καταστέλλοντας παράγοντες του ανοσιακού συστήματος, ώστε να περιοριστεί η εξάπλωση των καρκινικών κυττάρων και να προκληθεί η καταστροφή τους.
Υπό φυσιολογικές συνθήκες, τα κύτταρα του ανοσιακού μας συστήματος περιπολούν το σώμα μας, με σκοπό να προστατεύσουν τον οργανισμό από επικείμενες απειλές. Συγκεκριμένα, τα Τ λεμφοκύτταρα (Τ κύτταρα εν συντομία) του ανοσοποιητικού μας φέρουν στην επιφάνειά τους υποδοχείς, που είναι ικανοί να αναγνωρίζουν ξένους εισβολείς στον οργανισμό και να ενορχηστρώνουν επίθεση, με στόχο την καταπολέμησή τους. Τα ξένα μόρια ή ουσίες που αναγνωρίζονται από αυτούς τους υποδοχείς και μπορούν να προκαλούν ανοσολογική απάντηση ονομάζονται αντιγόνα. Κάθε αντιγόνο και υποδοχέας ταιριάζουν όπως ένα κλειδί σε μια κλειδαριά – κάθε συνδυασμός είναι μοναδικός, κάθε υποδοχέας αναγνωρίζει ένα συγκεκριμένο αντιγόνο και κάθε αντιγόνο αναγνωρίζεται από συγκεκριμένο υποδοχέα.
Πολλές φορές, το πρόβλημα με τα καρκινικά κύτταρα είναι πως τα επιφανειακά τους αντιγόνα δεν αναγνωρίζονται από αντίστοιχους υποδοχείς των ανοσιακών κυττάρων. Έτσι, δεν ενεργοποιείται εναντίον τους επίθεση, με αποτέλεσμα να επιβιώνουν και να πολλαπλασιάζονται στον οργανισμό. Ωστόσο, φαίνεται πως υπάρχει πλέον τρόπος αυτό το πρόβλημα να λυθεί μέσω μιας νέας μορφής ανοσοθεραπείας, με όνομα CAR T κύτταρα (Chimeric Antigen Receptor T cells). Η προσέγγιση αυτή περιλαμβάνει την αφαίρεση Τ κυττάρων από το αίμα του ασθενούς, την επεξεργασία τους στο εργαστήριο και την επαναχορήγησή τους στον ασθενή.
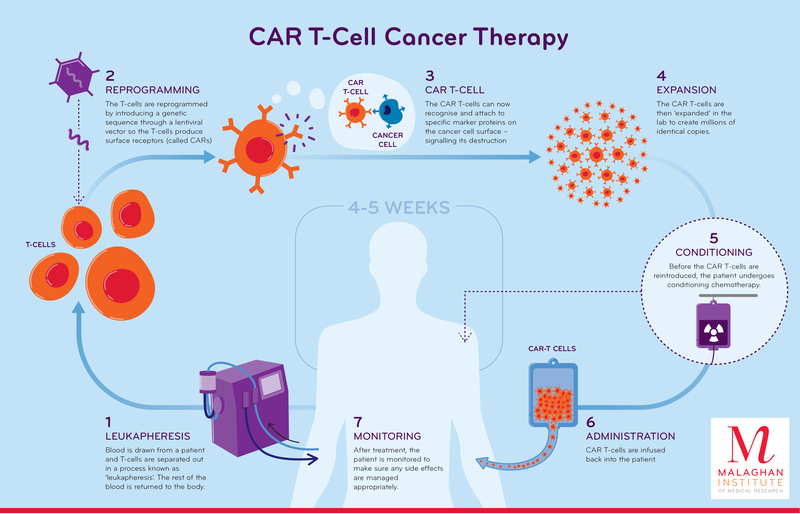
Κατά την επεξεργασία τους, εισάγεται σε αυτά ένα γονίδιο, ώστε να μπορέσουν να παράγουν και να εμφανίσουν στην επιφάνειά τους τον επιθυμητό υποδοχέα για κάποιο αντιγόνο των καρκινικών κυττάρων. Οι υποδοχείς αυτοί είναι συνθετικά μόρια και εξατομικεύονται για κάθε ασθενή, ανάλογα με τον τύπο του καρκίνου και το αντιγόνο-στόχο. Το γονίδιο με την πληροφορία για τον σχηματισμό τους εισάγεται στα κύτταρα με τη βοήθεια ενός ιού-φορέα, που έχει τροποποιηθεί. Με αυτόν τον τρόπο, είναι δυνατή η πυροδότηση ανοσιακής απάντησης έναντι των καρκινικών κυττάρων, ώστε να οδηγηθούν στην καταστροφή. Είναι πιθανό να προηγηθεί της επαναχορήγησής τους στον ασθενή χημειοθεραπευτικό σχήμα, ώστε να ενισχυθεί η αποτελεσματικότητα της θεραπείας.
Αφού καμία θεραπευτική προσέγγιση δεν είναι πανάκεια, η εφαρμογή των CAR T κυττάρων συνοδεύεται από ορισμένες επιπλοκές. Μια από τις συχνότερες και σοβαρότερες είναι το σύνδρομο απελευθέρωσης κυτταροκινών (CRS), το οποίο χαρακτηρίζεται από την υπερδιέγερση του ανοσιακού συστήματος και την υπερβολική φλεγμονογόνο δράση των εκλυόμενων παραγόντων. Τα συμπτώματά του είναι μη ειδικά, όπως πυρετός, ζάλη, κακουχία, μυαλγίες, αρθραλγίες, ναυτία, έμετος, αίσθημα παλμών και δύσπνοια, και για την αντιμετώπισή του χρησιμοποιούνται κορτικοστεροειδή και βιολογικοί παράγοντες. Άλλες επιπλοκές μπορεί να εμφανιστούν από το νευρικό σύστημα, με τη μορφή κεφαλαλγίας, σύγχυσης, επιληπτικών κρίσεων και διαταραχών ομιλίας, ισορροπίας ή συνείδησης. Ακόμα, υπάρχει η περίπτωση αλλεργικής αντίδρασης ή σοβαρής προσβολής από λοιμώξεις, λόγω πτώσης των λευκοκυττάρων στο αίμα.
Αν και τα πρώτα CAR T κύτταρα κατασκευάστηκαν στα τέλη της δεκαετίας του ‘80, μόλις το 2017 πήραν έγκριση από τον FDA για την αντιμετώπιση αιματολογικών κακοηθειών, όπως η λευχαιμία, τα λεμφώματα και το πολλαπλούν μυέλωμα. Αν και μέχρι στιγμής χρησιμοποιούνται κυρίως συμπληρωματικά σε ανθεκτικές μορφές των ασθενειών μετά από αποτυχία των αρχικών θεραπευτικών σχημάτων, νέες κλινικές μελέτες δείχνουν πως σε ορισμένες περιπτώσεις λειτουργούν αποτελεσματικότερα από την κλασική θεραπεία. Επιπλέον, εξετάζεται η χορήγησή τους σε παιδιατρικούς ασθενείς αυξημένου κινδύνου για υποτροπή, μετά την αρχική τους χημειοθεραπεία. Περαιτέρω έρευνα πιθανόν να συμβάλει στην καθιέρωση της χρήσης τους και την επέκτασή της και σε άλλα νεοπλασματικά νοσήματα.
ΕΝΔΕΙΚΤΙΚΕΣ ΠΗΓΕΣ
- CAR T Cell Therapy, Penn Medicine. Διαθέσιμο εδώ
- CAR T Cells: Engineering Patients’ Immune Cells to Treat Their Cancers, NIH. Διαθέσιμο εδώ
- CAR T-cell and Its Side Effects, American Cancer Society. Διαθέσιμο εδώ