Της Αγγελίνας Στύλα,
Τα μοντέλα που βασίζονται σε επαγόμενα πολυδύναμα βλαστοκύτταρα (iPSC) αποτελούν πολύτιμη πηγή για τη μελέτη μηχανισμών ασθενειών in vitro σε κυτταρικό επίπεδο. Από την εμφάνιση της τεχνολογίας iPSC πριν από μια δεκαετία, έχει σημειωθεί τεράστια πρόοδος στη βιολογία των βλαστοκυττάρων και στην αναγεννητική ιατρική. Τα ανθρώπινα iPSC έχουν χρησιμοποιηθεί ευρέως για μοντελοποίηση ασθενειών, ανακάλυψη φαρμάκων και ανάπτυξη κυτταρικής θεραπείας. Νέοι παθολογικοί μηχανισμοί έχουν αποσαφηνιστεί, νέα φάρμακα που προέρχονται από την κωδικοποίηση του μηχανισμού αυτού βρίσκονται σε εξέλιξη και έχει ξεκινήσει η πρώτη κλινική δοκιμή, που επιβεβαιώνει την επιτυχία της χρήσης βλαστοκυττάρων για την εύρεση θεραπειών δυσμενών ασθενειών, που ταλαιπωρούν πολλούς συνανθρώπους μας. Ποια είναι η λογική, όμως, του συγκεκριμένου μηχανισμού;
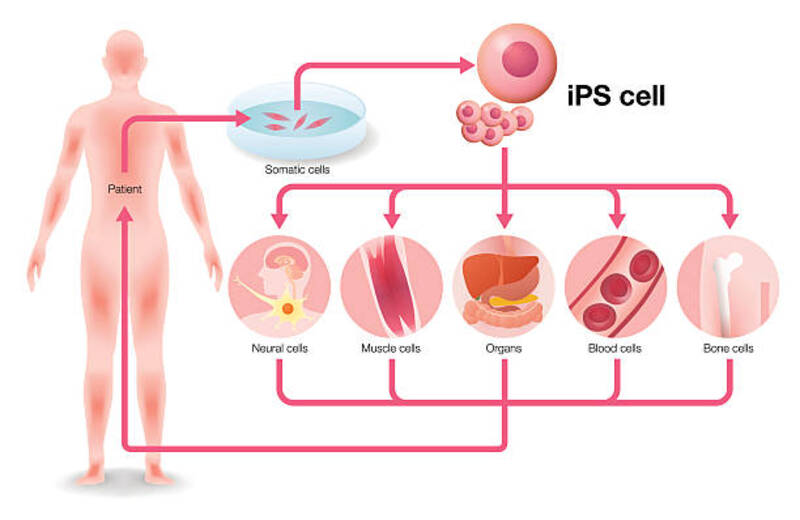
Τόσο τα ανθρώπινα ESC (εμβρυακά βλαστοκύτταρα) όσο και τα iPSC έχουν χρησιμοποιηθεί για τη μοντελοποίηση ανθρώπινων γενετικών ασθενειών. Η μοντελοποίηση με χρήση ανθρώπινων iPSC ξεκινά με την απομόνωση των iPSC από σωματικά κύτταρα ασθενών (π.χ. ινοβλάστες, Τ-λεμφοκύτταρα, κερατινοκύτταρα), τα οποία περιέχουν τις μεταλλάξεις που προκαλούν τη νόσο. Αυτά τα κύτταρα στη συνέχεια διαφοροποιούνται σε κυτταρικούς τύπους σχετικούς με την ασθένεια με τη χρήση κατάλληλων μεταγραφικών παραγόντων. Τα κύτταρα που προκύπτουν μετά τον επαναπρογραμματισμό των iPSC (όπως νευρώνες, καρδιομυοκύτταρα, κύτταρα παγκρέατος) χρησιμοποιούνται για την αποκάλυψη της αιτιολογίας της νόσου και τον εντοπισμό παθολογικών μηχανισμών που την προκάλεσαν. Σε πρώιμες μελέτες μοντελοποίησης ασθενειών που βασίζονται στο iPSC, αυτά που προέρχονται από άτομα, που δεν έχουν προσβληθεί από ασθένεια χρησιμοποιήθηκαν ως έλεγχοι για iPSC, που προέρχονται από ασθενείς.
Ωστόσο, όπως και άλλα κύτταρα, τα iPSC έχουν παρουσιάσει παραλλαγές, γεγονός που περιπλέκει την ερμηνεία των δεδομένων, λόγω μη σωστής διάκρισης της παραλλαγής από τους πραγματικούς φαινοτύπους που σχετίζονται με αυτή. Κάποιες από τις βασικές ασθένειες, στις οποίες χρησιμοποιήθηκε η συγκεκριμένη τεχνολογία για την αντιμετώπιση των δυσμενών επιπτώσεων τους, είναι νευρολογικές διαταραχές, με βασικό και πρόσφατο επιτυχόν παράδειγμα την επιληψία, ενώ τάσσονται σύμμαχοι των γιατρών στη μεγάλη μάχη κατά του καρκίνου.
Αναφορικά με ορισμένες αναπτυξιακές και επιληπτικές εγκεφαλοπάθειες, όπως το σύνδρομο Dravet (μυοκλονική επιληψία βρεφικού τύπου), η μοντελοποίηση της επιληψίας με iPSCs επιτρέπει την ανάπτυξη νέων φαρμάκων, έχοντας ως βάση τους διευκρινισμένους παθομηχανισμούς. Για τον σκοπό αυτό, τα βλαστοκύτταρα επαναπογραμματίζονται προς νευρώνες, αναπαριστώντας το 2D δίκτυο αλληλεπιδράσεων τους και συγκρίνοντάς το με το αντίστοιχο των υγειών, που χρησιμοποιήθηκαν ως έλεγχος για την εύρεση της αιτιολογίας της νόσου. Επιπλέον, η μεταμόσχευση νευρωνικών κυττάρων που προέρχονται από iPSC στον εγκέφαλο έχει μεγάλες δυνατότητες για τη θεραπεία ανθεκτικών επιληψιών. Οι πρόσφατες εξελίξεις στην τεχνολογία iPSC επέτρεψαν τη δημιουργία νευρωνικών οργανοειδών ή «μίνι εγκεφάλων». Αυτά τα οργανοειδή επιδεικνύουν ηλεκτροφυσιολογικές δραστηριότητες παρόμοιες με αυτές του εγκεφάλου και έχουν τη δυνατότητα για εκτεταμένες ευκαιρίες έρευνας για την επιληψία.
Αναφορικά με τη δημιουργία καρκινικών iPSC, τα καρκινικά κύτταρα μπορούν να απομονωθούν από τον όγκο και να διαφοροποιηθούν σε καρκινικά-iPSC με επαναπρογραμματισμό πολυδύναμων παραγόντων in vitro. Αυτά τα κύτταρα έχουν ικανότητα αθανασίας και πολλαπλασιασμού και μπορούν να δημιουργήσουν όγκους και με τις κατάλληλες αναλύσεις να βρεθεί η παθοφυσιολογία της νόσου.
Σε επιπλέον εφαρμογές, η αναγεννητική θεραπεία με βάση το iPSC έχει διαδοθεί ευρέως ως ένα νέο μέσο για τη βελτίωση της λειτουργίας εκφυλισμένων οργάνων λόγω της γήρανσης, όπως η ηλικιακή εκφύλιση της ωχράς κηλίδας, η γενετική προδιάθεση, ο τραυματισμός και οι χημειοθεραπείες. Η πρώτη κλινική δοκιμή για τη θεραπεία της γενεάς ωχράς κηλίδας (AMD) που σχετίζεται με την ηλικία με αυτόλογα επιθηλιακά κύτταρα χρωστικής αμφιβληστροειδούς, που προέρχονται από iPSC ξεκίνησε το 2014 στην Ιαπωνία.

Στις πρώτες ενέργειες σχετικά με την παραγωγή iPSC από τον ποντικό και τον άνθρωπο, χρησιμοποιήθηκαν είτε ρετροϊικοί φορείς είτε φακοϊοί για τη χορήγηση γονιδίων Oct4, Sox2, Klf4 και c-Myc (Yamanaka μεταγραφικοί παράγοντες) σε σωματικά κύτταρα. Η αποτελεσματικότητα της μεταγωγής με ρετροϊούς είναι αρκετά υψηλή, αν και δεν είναι η ίδια για διαφορετικούς τύπους κυττάρων. Συνεπώς, το πρόβλημα που προκύπτει είναι ότι η ενσωμάτωση του ρετροϊού στο γονιδίωμα του ξενιστή απαιτεί ένα συγκριτικά υψηλό ποσοστό διαίρεσης, το οποίο είναι χαρακτηριστικό του σχετικά στενού φάσματος των καλλιεργημένων κυττάρων.
Ένα άλλο σοβαρό πρόβλημα περιλαμβάνει το ίδιο το γονιδιακό σύνολο που χρησιμοποιείται για την επαγωγή πολυδυναμίας. Η έκτοπη μεταγραφή των Yamanaka μπορεί να οδηγήσει σε νεοπλασματική ανάπτυξη από κύτταρα που προέρχονται από iPSC, επειδή η έκφραση των γονιδίων από τη φύση τους, σχετίζεται με την ανάπτυξη πολλαπλών όγκων.
Ανακεφαλαιώνοντας, η iPSC είναι μια προηγμένη τεχνολογία που έχει χρησιμοποιηθεί στην αντιμετώπιση τραυμάτων μυών και οστών, την επούλωση πληγών και εγκαυμάτων, καθώς και τη θεραπεία διαφόρων παθήσεων όπως η επιληψία, ο σακχαρώδης διαβήτης και ο καρκίνος. Επίσης, η τεχνολογία αυτή έχει ανοίξει νέους δρόμους στον τομέα της μελέτης της αναγέννησης των ιστών και της αντικατάστασης αυτών, που έχουν υποστεί ζημιά. Ωστόσο, υπάρχουν ακόμα ορισμένα εμπόδια που περιορίζουν την ασφαλή της χρήση και πρέπει με διάφορα μέτρα ασφαλείας να αντιμετωπιστούν για να επωμιστούμε στο έπακρο τα οφέλη της εν λόγω τεχνικής.
ΕΝΔΕΙΚΤΙΚΕΣ ΠΗΓΕΣ
- Current Challenges of iPSC-Based Disease Modeling and Therapeutic Implications, mdpi.com. Διαθέσιμο εδώ
- Induced pluripotent stem cell technology: a decade of progress – PMC, nature reviews drug discovery, nature.com. Διαθέσιμο εδώ
- Cancer cells as a new source of induced pluripotent stem cells Stem cell research and therapy, biomedcentral.com. Διαθέσιμο εδώ
- Induced Pluripotent Stem Cells: Problems and Advantages when Applying them in Regenerative Medicine, National Institutes of Health (NIH). Διαθέσιμο εδώ