Του Αλέξανδρου Κομπή,
Οι περισσότερες χημικές διεργασίες που επιτελούνται στον οργανισμό μας και κατ’ επέκταση στα ίδια τα κύτταρά μας, πραγματοποιούνται με τη βοήθεια ενός ή περισσότερων ενζύμων. Τα ένζυμα διαδραματίζουν σπουδαίο ρόλο στα στάδια του μεταβολισμού, καθώς αφενός καταλύουν τις χημικές αντιδράσεις και αφετέρου, σε ορισμένες περιπτώσεις, αποτελούν στοιχεία ρύθμισης της ενεργητικότητας και της ταχύτητας του μεταβολισμού ανάλογα με τις ανάγκες του κυττάρου την εκάστοτε στιγμή. Για αυτόν τον λόγο, η απουσία ή η δυσλειτουργία ενός ή περισσότερων ενζύμων μπορεί να διαταράξει την ομαλή λειτουργία των κυττάρων και να προκαλέσει σοβαρά προβλήματα υγείας. Μια από τις σημαντικότερες και πιο διαδεδομένες ενζυμοπάθειες, η οποία ταυτόχρονα έχει και ένα ιδιαίτερο κλινικό ενδιαφέρον, είναι η ανεπάρκεια της αφυδρογονάσης της 6-φωσφορικής γλυκόζης ή, όπως καλείται εν συντομία, ανεπάρκεια G6PD. Σε ορισμένες βιβλιογραφικές πηγές, η εν λόγω ανεπάρκεια αναφέρεται και ως κυαμισμός ή φαβισμός.
Το ένζυμο αφυδρογονάση της 6-φωσφορικής γλυκόζης (G6PD), κωδικοποιείται από το γονίδιο G6PD, που εδράζεται στο Χ φυλετικό χρωμόσωμα. Το συγκεκριμένο ένζυμο, φυσιολογικά, βρίσκεται στο κυτταρόπλασμα όλων των κυττάρων του σώματός μας και συμμετέχει στη μεταβολική πορεία των φωσφορικών πεντοζών. Το μεταβολικό μονοπάτι αυτών αποτελεί την κύρια πηγή νικοτιναμιδο-αδενινο-δινουκλεοτίδιου (NADPH), το οποίο είναι ένα απαραίτητο συστατικό-μόριο για τη βιοσύνθεση των λιπαρών οξέων, των νουκλεοτιδίων καθώς και άλλων βιολογικών μακρομορίων. Επιπλέον, το NADPH συμμετέχει στην προστασία των κυττάρων, και ειδικότερα των ερυθρών αιμοσφαιρίων, από το οξειδωτικό στρες.
Στο σημείο αυτό θα πρέπει να τονίσουμε ότι το οξειδωτικό στρες που υφίστανται τα κύτταρα προκαλείται από διάφορες αντιδραστικές χημικές ενώσεις οξυγόνου (ROS), οι οποίες παράγονται φυσιολογικά από τον οξειδωτικό μεταβολισμό των ίδιων των κυττάρων, είτε προσλαμβάνονται εξωγενώς (διατροφή, φαρμακευτικές ουσίες) και δυνητικά μπορεί να δημιουργήσουν προβλήματα στο κύτταρο, επιφέροντας εν τέλει την καταστροφή του. Τα κύτταρα που επηρεάζονται περισσότερο από το οξειδωτικό στρες είναι τα ερυθρά αιμοσφαίρια, λόγω της ενδογενούς παρουσίας αυξημένων επιπέδων αντιδραστικών χημικών ενώσεων οξυγόνου. Παρόλα αυτά, υπό φυσιολογικές συνθήκες, οι αντιδραστικές ενώσεις οξυγόνου διατηρούνται σε χαμηλά επίπεδα μέσω ενός μηχανισμού, ο οποίος χρησιμοποιεί το NADPH. Αυτό αποτελεί ένα από τα απαραίτητα στοιχεία για τη σωστή λειτουργία του μηχανισμού απενεργοποίησης των αντιδραστικών χημικών ενώσεων οξυγόνου. Συνεπώς, η μείωση των επιπέδων του εντός των κυττάρων έχει σοβαρό αντίκτυπο και μπορεί να οδηγήσει σε εκτεταμένη καταστροφή των ερυθρών αιμοσφαιρίων (αιμόλυση). Η κύρια αιτία χαμηλών επιπέδων NAPDH είναι η ανεπάρκεια G6PD, η οποία μειώνει την ενεργότητα του μονοπατιού των φωσφορικών πεντοζών και συνεπώς, καθορίζει έμμεσα τα επίπεδά του.
Η ανεπάρκεια G6PD είναι μια γενετική φυλοσύνδετη κληρονομική ασθένεια, η οποία εμφανίζεται σε μεγαλύτερο ποσοστό στα αρσενικά άτομα απ’ ό,τι στα θηλυκά, και οφείλεται σε μεταλλάξεις του γονιδίου G6PD. Οι μεταλλάξεις αυτές έχουν ως αποτέλεσμα τη δημιουργία ενός δυσλειτουργικού ενζύμου G6PD ή την παραγωγή ανεπαρκούς ποσότητας φυσιολογικού ενζύμου. Ως εκ τούτου, η παραγωγή NADPH, μέσω της οδού των φωσφορικών πεντοζών, μειώνεται σημαντικά και τα επίπεδά του στο εσωτερικό των κυττάρων δεν είναι επαρκούν, ώστε να αντιρροπίσουν τη δράση των ενδογενών, αλλά και των εξωγενών δραστικών ριζών οξυγόνου. Συνεπώς, τα ερυθρά αιμοσφαίρια καθίστανται εξαιρετικά επιρρεπή σε αιμόλυση. Η συμπτωματολογία της ασθένειας ποικίλλει ανάλογα με την ηλικία και το είδος της μετάλλαξης. Σε γενικές γραμμές, όμως, στις περισσότερες των περιπτώσεων παρουσιάζεται αιμολυτική αναιμία. Εντούτοις, η κλασική συμπτωματολογία της ασθένειας δεν εμφανίζεται πάντα, και στην πλειοψηφία τους οι άνθρωποι που πάσχουν παραμένουν ασυμπτωματικοί. Το γεγονός αυτό έχει άμεσο συσχετισμό με τη σοβαρότητα και τον χαρακτήρα των μεταλλάξεων. Ορισμένες μεταλλάξεις προκαλούν έντονη συμπτωματολογία, ενώ άλλες απαιτούν τη λήψη εξωγενούς πηγής ριζών οξυγόνου για να προκαλέσουν συμπτώματα. Τέτοιες εξωγενείς πηγές είναι τρόφιμα, όπως τα κουκιά και άλλα όσπρια, καθώς και φαρμακευτικές ουσίες, όπως ορισμένα αντιβιοτικά και ανθελονοσιακά σκευάσματα.

Η διάγνωση της ασθένειας βασίζεται στην κλινική εξέταση, στη συμπτωματολογία, στη λήψη ιστορικού και σε εξειδικευμένες εργαστηριακές εξετάσεις που βασίζονται σε αιματολογικές παραμέτρους. Επίσης, τα τελευταία χρόνια, έχει ενταχθεί στην κλινική πράξη ο εργαστηριακός έλεγχος των νεογνών, στα πλαίσια της διάγνωσης και, μάλιστα, με υψηλά ποσοστά επιτυχίας. Όσον αφορά τις θεραπευτικές προσεγγίσεις, αυτές προσανατολίζονται προς δύο κατευθύνσεις. Από την μια πλευρά, οι ασθενείς θα πρέπει να αποφεύγουν την κατανάλωση τροφίμων που περιέχουν οξειδωτικούς παράγοντες και τη λήψη φαρμάκων που θα μπορούσαν να πυροδοτήσουν ένα επεισόδιο αιμόλυσης, ενώ από την άλλη, οι ασθενείς που εμφανίζουν αιμολυτικά επεισόδια, χωρίς την κατανάλωση κάποιας πηγής οξειδωτικών ενώσεων, κρίνεται απαραίτητο να υπόκεινται σε συχνές μεταγγίσεις αίματος.
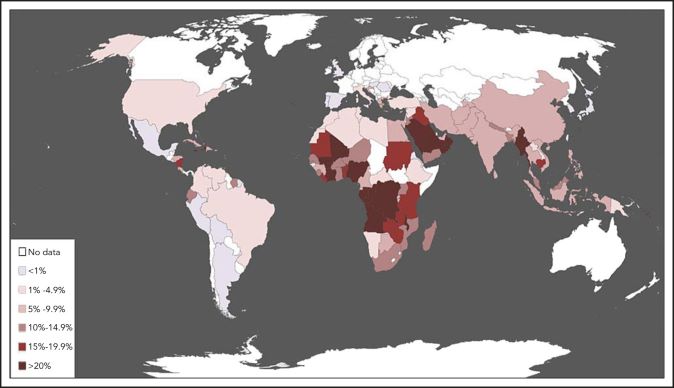
Στατιστικά μιλώντας, η ανεπάρκεια G6PD είναι από τις πλέον διαδεδομένες ενζυμοπάθειες και υπολογίζεται ότι πάνω από 400 εκατομμύρια άνθρωποι πάσχουν παγκοσμίως. Παρόλα αυτά, η εμφάνιση της νόσου παρουσιάζει ανομοιόμορφη κατανομή ανά τον κόσμο, με τα περισσότερα περιστατικά να σημειώνονται σε τροπικές και υποτροπικές περιοχές. Πιο συγκεκριμένα, ο μεγαλύτερος επιπολασμός της ασθένειας καταγράφεται σε χώρες της Αφρικής, της Μεσογείου και της Νότιας Ασίας. Η υψηλή συχνότητα εμφάνισης στις περιοχές αυτές σχετίζεται άμεσα με τη συχνότητα εμφάνισης της ελονοσίας ως ενδημικού λοιμώδους νοσήματος. Ως γνωστόν, η ελονοσία είναι μια ασθένεια η οποία οφείλεται στο πλασμώδιο, μεταδίδεται μέσω των κουνουπιών και ενδημεί κυρίως στις προαναφερθείσες περιοχές. Ο συσχετισμός μεταξύ της υψηλής συχνότητας εμφάνισης ελονοσίας και της ανεπάρκειας G6PD στις συγκεκριμένες γεωγραφικές περιοχές, οφείλεται στο εξελικτικό πλεονέκτημα επιβίωσης που προσδίδει η ανεπάρκεια G6PD. Ουσιαστικά, η ανεπάρκεια G6PD προστατεύει από την ελονοσία με έναν έμμεσο τρόπο. Το πλασμώδιο που προκαλεί την ελονοσία απαιτεί υψηλά επίπεδα NADPH για να πολλαπλασιαστεί μέσα στα ερυθρά αιμοσφαίρια και να προκαλέσει λοίμωξη. Τα άτομα που πάσχουν από ανεπάρκεια έχουν σοβαρή έλλειψη NADPH, με αποτέλεσμα να εμφανίζουν εγγενή ανθεκτικότητα στη λοίμωξη από πλασμώδιο. Η ιδιαιτερότητα αυτή τους προσδίδει μεγαλύτερη πιθανότητα επιβίωσης σε σχέση με του υγιείς και, για αυτόν τον λόγο, εντοπίζονται εκτενώς σε περιοχές που κυριαρχεί η ελονοσία.
Η ανακάλυψη του κυαμισμού ή φαβισμού πριν από 70 χρόνια, περίπου, έφερε στο φως νέα δεδομένα και μπόρεσε να ερμηνεύσει περιπτώσεις, στις οποίες φαινομενικά υγιείς άνθρωποι παρουσίαζαν ασυνήθιστα συμπτώματα ύστερα από τη λήψη ορισμένων τροφίμων και φαρμακευτικών ουσιών. Επιπροσθέτως, η σπουδαία αυτή ανακάλυψη άνοιξε τον δρόμο για την αναζήτηση αποτελεσματικών θεραπειών και τη διαμόρφωση ενός προτύπου διαβίωσης, το οποίο θα βασιζόταν σε επίπεδο διατροφής και επιλεκτικής λήψης φαρμάκων, έτσι ώστε να αποφευχθούν οι επικίνδυνές εκδηλώσεις της ασθένειας. Τέλος, αξίζει να αναφερθεί πως τα τελευταία χρόνια, με την ανάπτυξη της γενετικής και την αποκωδικοποίηση του ανθρώπινου γονιδιώματος, εξετάζονται νέες θεραπείες, οι οποίες θα στοχεύουν σε γενετικό επίπεδο και θα αποτελούν μια πρωτοποριακή λύση για την αντιμετώπιση του προβλήματος.
ΕΝΔΕΙΚΤΙΚΕΣ ΠΗΓΕΣ
- Jeremy M. Berg, John L. Tymoczko, Gregory J. Gatto Jr, Lubert Stryer, Bιοχημεία, 8η έκδοση, Πανεπιστημιακές Εκδόσεις Κρήτης, Κρήτη, 2015.
- S. Russ Richardson Gerald F. O’Malley (2021), Glucose 6 Phosphate Dehydrogenase Deficiency, StatPearls Publishing. Διαθέσιμο εδώ
- Lucio Luzzatto, Mwashungi Ally, Rosario Notaro (2020), Glucose-6-phosphate dehydrogenase deficiency, Blood, Volume 136, Issue 11, pages1225-1240. Διαθέσιμο εδώ
- Glucose-6-phosphate dehydrogenase deficiency, rarediseases.info.nih.gov. Διαθέσιμο εδώ




